#1 Acidose metabólica e resistência à insulina
Acidose metabólica de baixo grau como fator de resistência à insulina
A acidose metabólica é uma condição crônica que muitas pessoas no mundo ocidental têm, mas não percebem. [*] Nesse artigo eu vou escrever sobre como podemos reconhecer clinicamente a acidose metabólica de baixo grau como fator de resistência a insulina. Este artigo será escrito baseado e adaptado dos estudos de James J DiNicolantonio e publicado na revista científica BMJ.
Resumo dos efeitos da acidose na resistência à insulina
-
A indução experimental de acidose metabólica em humanos prejudica o metabolismo da glicose e a sensibilidade celular à insulina. [32]
-
A correção da acidose metabólica em humanos melhora a sensibilidade à insulina.[31]
-
A acidose metabólica reduz a ligação da insulina aos receptores nos adipócitos e induz a resistência à insulina no músculo [14,34,35]
-
A acidose metabólica aumenta a produção de cortisol, o que reduz a sensibilidade à insulina no músculo esquelético e nas células adiposas.[26]
-
A acidose metabólica leve reduz a ligação da insulina ao seu receptor e a sinalização intracelular da insulina a jusante nos mioblastos e adipócitos.[14,35,39]
-
Um pH baixo diminui a expressão do sensibilizador de insulina adiponectina, [40] que é um hormônio que melhora a sensibilidade à insulina do músculo esquelético. [26,41]
-
A secreção de leptina é regulada negativamente em adipócitos expostos a um pH médio baixo, enquanto a administração de bicarbonato de sódio a pessoas com acidose induzida por rins aumenta os níveis séricos de leptina.[45,46]
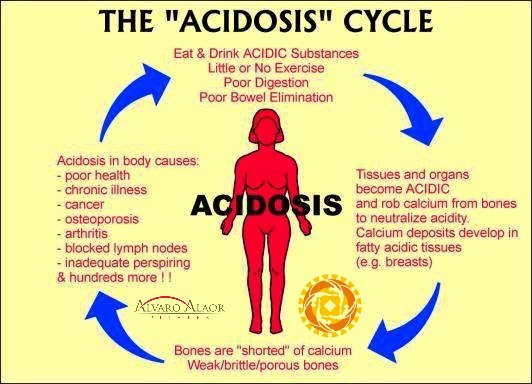
O que é acidose metabólica e como se desenvolve?
Já escrevi a respeito da acidose metabólica em outro artigo, mas aqui vamos tratar de como a acidose afeta a resistência a insulina.
A acidose metabólica ocorre quando há retenção de ácido no corpo, o que leva a uma queda na capacidade de tamponamento de ácido do corpo. No entanto, a retenção ácida pode ocorrer mesmo quando o bicarbonato sérico é normal. [1] Existem quatro mecanismos pelos quais o corpo pode desenvolver acidose metabólica: (1) aumento da ingestão de ácido dietético, (2) aumento da produção de ácido fixo, como na cetoacidose diabética, cetoacidose alcoólica ou jejum prolongado, (3) aumento da perda de base (ou seja, diarreia) e (4) redução da excreção renal de ácido. Além disso, medicamentos específicos podem causar ou contribuir para a acidose metabólica.
Existem dois tipos principais de ácido no corpo, ácido carbônico e ácido não carbônico. O ácido carbônico é formado quando uma molécula de bicarbonato se combina com um íon hidrogênio. Eventualmente, o ácido carbônico é transformado em água e dióxido de carbono. Assim, se criarmos bicarbonato no corpo a partir da alcalinidade fornecida pela dieta, podemos expirar o ácido sem esgotar nossos próprios níveis de bicarbonato.
Os ácidos não carbônicos são ácidos fixos e não podem ser exalados pelos pulmões. Eles incluem ácido lático, ácido fosfórico, ácido sulfúrico, ácido úrico e os cetoácidos ácido acetoacético e ácido beta-hidroxibutírico. Alguns desses ácidos fixos podem ser excretados na urina em sua forma livre, no entanto, o pH da urina só pode cair para cerca de 4,4 e, portanto, apenas quantidades insignificantes de ácidos fortes, como o ácido sulfúrico, podem ser eliminadas em sua forma titulável livre.[2]
Assim, 99% das vezes o ácido sulfúrico deve ser transformado em íons de hidrogênio e sulfato e então pode ser eliminado pelo organismo.
Quando comemos proteína animal rica em aminoácidos contendo enxofre, como metionina, cisteína e taurina, formamos ácido sulfúrico, que é dividido em dois íons de hidrogênio e uma molécula de sulfato. Se consumirmos uma grande quantidade de proteína animal, isso leva à produção de grandes quantidades de íons de hidrogênio, que são neutralizados por citrato ou bicarbonato.
Assim, consumir grandes quantidades de proteína animal esgota nossa capacidade de tamponamento de bicarbonato e citrato.
Isso pode se tornar especialmente problemático quando começamos a produzir mais de 40 a 70 mEq de ácido por dia, o que normalmente ocorre em um pH urinário de 6,25 a 6,5. Assim, se o pH urinário for 6,5 ou menos, isso sugere retenção ácida e risco de desenvolver acidose metabólica de baixo grau. É por isso que eu disponibilizo o exame rápido de urina para meus clientes, e eu mesmo faço diariamente, para eu ter ideia de meu equilíbrio ácido/base diário, uma variação metabólica com meus hábitos de vida. Porém maioria das pessoas ainda estão condicionadas ao exame de laboratório e não entendem monitorização de saúde de rotina.
Quando o ácido sulfúrico é formado no corpo, os íons de hidrogênio devem ser neutralizados via bicarbonato.
Adicionalmente, o sulfato carregado negativamente deve ser eliminado, o que requer que uma molécula carregada positivamente seja excretada para fora do corpo. Normalmente, isso significa que minerais carregados positivamente como magnésio, cálcio, sódio ou potássio são eliminados pela urina com o sulfato carregado negativamente, o que tende a esgotar o corpo de minerais.
O ácido sulfúrico tem uma estrutura molecular de H 2 SO 4 . Os dois íons de hidrogênio são neutralizados por duas moléculas de bicarbonato (ou três íons de hidrogênio podem ser neutralizados por uma molécula de citrato), o que deixa o sulfato remanescente. Como não podemos expirar o sulfato, ele deve ser excretado pelos rins. No entanto, para manter a eletroneutralidade, o sulfato carregado negativamente (SO4 2-) deve ser combinado com uma substância carregada positivamente.
Se a dieta contém minerais alcalinos suficientes, como magnésio, cálcio, sódio ou potássio, o sulfato pode ser excretado com os cátions da dieta. No entanto, se a dieta estiver carente desses minerais, o corpo perderá minerais até que os rins possam aumentar a produção de amônia para eliminar o sulfato. Por exemplo, dois íons de hidrogênio carregados positivamente (2H+) são produzidos nos rins para combinar com duas moléculas de amônia (2 NH3) formando 2 NH4+. Isso fornece a carga 2+ para compensar a carga 2− do sulfato para formar sulfato de amônio neutro (NH 4 SO 4 ) para excreção.
No entanto, o músculo e o tecido conjuntivo são QUEBRADOS para formar a amônia para eliminar o sulfato.
Além disso, uma vez que a capacidade dos rins de excreção de ácido é atingida, a eliminação de sulfato usando íons de hidrogênio e amônia diminui, exigindo uma maior dependência de minerais alcalinos. Também leva TEMPO para os rins sintetizarem amônia para excretar sulfato, assim, minerais alcalinos também serão excretados até que os rins possam aumentar a produção de amônia.
Assim, o estado ácido-base no corpo é um ato de equilíbrio determinado pela carga geral de ácido da dieta, Em outras palavras a capacidade dos rins de eliminar ácido depende a ingestão dietética de minerais alcalinos e substâncias formadoras de bicarbonato.
Consumir uma dieta rica em proteína animal, mas insuficiente em minerais alcalinos e substâncias formadoras de bicarbonato pode ESGOTAR o estado mineral do corpo, predispor à DEGRADAÇÃO ÓSSEA, MUSCULAR e do TECIDO CONJUNTIVO e, eventualmente, levar a DANOS aos rins.
É por isso que consumir água mineral bicarbonatada e/ou alimentos vegetais e minerais alcalinos, no contexto de uma dieta de base animal ou onívora, é um passo importante para manter o estado ácido-base do organismo. Assim, há um custo para comer uma dieta rica em proteína animal relacionada à produção de mais amônia (que induz danos musculares, do tecido conjuntivo e dos rins) e/ou perder mais minerais alcalinos (via degradação óssea).
Na dieta moderna, a lenta acidificação do corpo ocorre principalmente pelo consumo proporcionalmente alto de proteína animal e grãos em comparação com as frutas e vegetais que fornecem base. Além disso, bebidas contendo ácido fosfórico (refrigerantes carbonatados) também contribuem para a carga ácida da dieta.
Quando consumimos ânions orgânicos encontrados em frutas e vegetais, como citrato, malato e gluconato, eles podem se converter em bicarbonato no corpo e aceitar íons de hidrogênio para excreção. É assim que preservamos nossa capacidade de buffer. Quanto mais proteínas comemos, ou quanto mais músculos temos, mais ácido podemos excretar na urina como amônio. [2]
Consumir proteína adequada e construir/manter músculos robustos é importante para a saúde porque ajuda a reduzir o risco de sarcopenia, quedas e fragilidade, e cria mais reservas musculares e ósseas para eliminar o ácido extra. No entanto, ainda há um impacto negativo nos rins pelo aumento da produção de amônia para eliminar os íons hidrogênio e sulfato provenientes da proteína animal.
Estudos de equilíbrio de 1966 mostraram que humanos saudáveis consumindo dietas que produzem > 0,4 a 1 mEq de ácido/kg de peso corporal levam à retenção de ácido no corpo. [3] Para um adulto saudável médio, consumir uma dieta que leve a 40–70 mEq ou mais de produção líquida de ácido endógeno levará à retenção de ácido. [3]
Isso significa que a maioria dos americanos, brasileiros e ocidentais em sua maioria, estão consumindo dietas que provavelmente resultarão em alguma retenção de ácido – desencadeando a produção de grandes quantidades de amônia e outras consequências adversas à saúde, como cálculos renais, perda de músculos, perda de tecido conjuntivo e quebra óssea, pressão alta, resistência à insulina , dor crônica e outros problemas de saúde. [4,5,6] A acidose metabólica também aumenta o fluxo plasmático renal e a taxa de filtração glomerular para aumentar a excreção da carga ácida. [7,8,9] Efeitos semelhantes foram observados comendo refeições ricas em carne ou dietas carnívoras. [10,11]
Os rins podem até hipertrofiar devido ao aumento da produção de amônia. [12] Assim, ingerir uma alta carga ácida na dieta pode ser prejudicial aos rins.
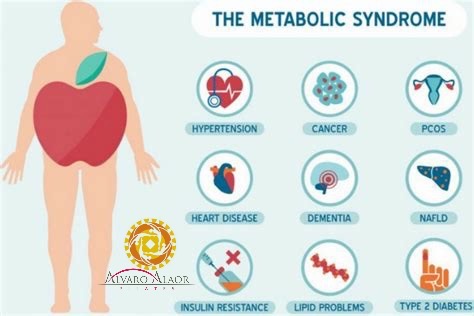
Acidose metabólica causa resistência à insulina e síndrome metabólica
O pH do fluido intersticial nos tecidos metabólicos muda prontamente e pode contribuir para o aparecimento da resistência à insulina através da diminuição da afinidade da insulina pelo seu receptor.’ [13]
Há uma capacidade de tamponamento diminuída no líquido intersticial em comparação com o citosol intracelular e o sangue. Isso se deve ao fato de que o interstício possui apenas tampões de pH relativamente fracos, como bicarbonato e fosfato, enquanto o sangue também possui proteínas como hemoglobina e albumina que podem se ligar a íons de hidrogênio.
Assim, o pH intersticial varia mais do que o sangue. A acidificação do fluido intersticial pode reduzir a ligação da insulina ao receptor de insulina e REDUZIR a captação de glicose na célula. [5,13,14]
De fato, o nível de lactato circulante, que sugere retenção de ácido na célula e no interstício, correlaciona-se negativamente com o grau de sensibilidade à insulina em humanos. [15,16] Estudos em ratos também mostram que o pH mais baixo do líquido intersticial ocorre na ascite e nos tecidos metabólicos antes do desenvolvimento dos sintomas diabéticos. [17]. Isso mostra que o exame de sangue não é um padrão tão fidedigno, o problema ja esta ocorrendo a nível celular e o sangue ainda não acusa.
O baixo pH urinário também está associado à pior resistência à insulina. [18,19] É importante ressaltar que em pacientes com síndrome metabólica, o pH da urina de 24 horas é significativamente menor do que em pessoas normais e correlaciona-se negativamente com o número de anormalidades da síndrome metabólica. [19]. E isso mostra a importância de fazermos exame rápido de urina.
Em resumo, a acidose metabólica de baixo grau predispõe à resistência à insulina, diabetes tipo 2 e síndrome metabólica.
Ácidos orgânicos fracos dietéticos (como ácido cítrico e acético) de frutas cítricas, ameixas, vinagre, etc. dissociam-se em ânions e prótons e apenas os ânions são absorvidos do lúmen intestinal para a circulação. Portanto, consumir ácidos orgânicos fracos melhora a capacidade de tamponamento de pH do corpo. [5,13].
A acidose metabólica piora a captação de glicose, oxidação e resistência à insulina
‘Acidose, com pH reduzido e ‘reserva alcalina’ dos fluidos corporais, tem vários efeitos secundários concomitantes. Esses efeitos interdependentes incluem distúrbios nas atividades normais dos sistemas enzimáticos que estão envolvidos em muitas fases do metabolismo de carboidratos e minerais, inibição da ação da insulina, aumento do catabolismo e diminuição do anabolismo nos tecidos.’ [20] ~ George M. Guest et al, 1952
Numerosos estudos mostram que a carga ácida da dieta está associada ao agravamento da sensibilidade à insulina e a um risco aumentado de diabetes tipo 2. [21,24] Níveis mais baixos de bicarbonato (um marcador de acidose metabólica de baixo grau) estão independentemente associados à redução da sensibilidade à insulina. [25]
Em participantes saudáveis do National Health and Nutrition Examination Surveys 1999–2002, indivíduos com bicarbonato sérico <22 mmol/L tiveram insulina em jejum 12,7 pmol/L maior do que aqueles com nível >25 mmol/L. O valor médio para os níveis de bicarbonato foi de 23 mmol/L, sugerindo que a maioria das pessoas saudáveis nos Estados Unidos tem acidose metabólica de baixo grau (bicarbonato sérico < 24–26 mmol/L). [25]
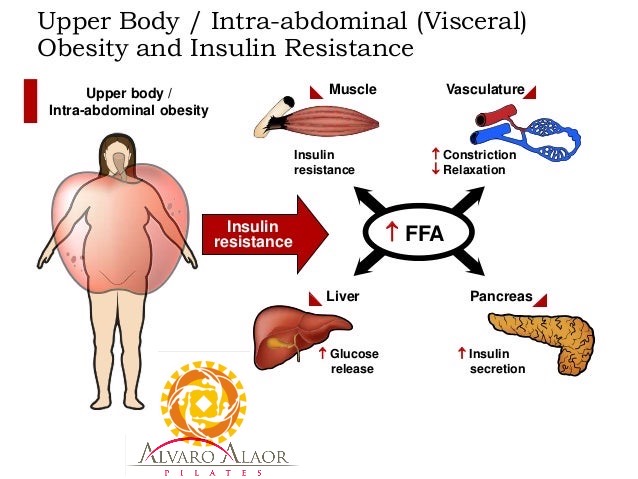
Ter um pH urinário baixo, outro marcador de acidose metabólica de baixo grau, está associado a um maior risco de OBESIDADE VICERAL e SÍNDROME METABÓLICA. [18] Uma alta carga ácida na dieta também aumenta o cortisol, que pode causar adiposidade visceral e aumentar a glicemia e a pressão arterial. [26,30]
Estudos clínicos mostram que a correção da acidose metabólica melhora a sensibilidade à insulina. [31] A indução experimental de acidose metabólica em humanos prejudica o metabolismo da glicose e a sensibilidade celular à insulina. [32] A acidose é um potente inibidor da fosfofrutoquinase, a enzima limitante da taxa de glicólise. [33]
Além disso, a acidose reduz a ligação da insulina aos receptores nos adipócitos, [34,35] e induz a resistência à insulina no músculo [14] e reduz a sensibilidade à insulina no músculo esquelético e nas células adiposas, aumentando a produção de cortisol. [26]
Um pH baixo estimula a secreção de cortisol para aumentar a depuração (elimienção) plasmática do excesso de íons hidrogênio. [27,28] Uma maior carga ácida da dieta está associada a maiores concentrações de cortisol e/ou seus marcadores urinários. [29] Em contraste, a suplementação alcalina diminui os níveis de cortisol, a secreção total de glicocorticóides adrenais e glicocorticóides livres potencialmente bioativos. [36,37]
Assim, a acidose metabólica induz resistência à insulina e eleva os níveis de cortisol, enquanto a correção da acidose por meio de terapias alcalinas melhora esses marcadores.
A administração de ácido dietético na forma de cloreto de amônio a ratos normais ou ratos diabéticos levemente acidóticos leva à perda quase total da resposta à insulina devido à inibição do receptor de insulina e da glicólise, que é revertida com a suplementação de bicarbonato de sódio. [38] A ligação da insulina nos adipócitos é reduzida em ratos cetoacidóticos e as infusões de cloreto de amônio reduzem os receptores de insulina nos adipócitos, o que é melhorado com infusões de bicarbonato de sódio. [35]
A acidose metabólica leve reduz a ligação da insulina ao seu receptor e a sinalização intracelular da insulina a jusante nos mioblastos e adipócitos. [14,35,39] Os autores de um estudo concluíram: ‘Nosso presente estudo sugere que condições de pH extracelular reduzido podem produzir a patogênese da resistência à insulina nas células do músculo esquelético.‘ [14]
Uma consequência disso pode ser a degradação acelerada de proteínas no músculo esquelético. [39] ou seja perda de massa muscular. Além disso, um pH baixo diminui a expressão do sensibilizador de insulina adiponectina, [40] que é um hormônio que melhora a sensibilidade à insulina do músculo esquelético. [26,41]
Portanto, através da redução da sinalização da adiponectina e da insulina, a acidose metabólica pode induzir a resistência à insulina. No entanto, a leptina, que é um hormônio da saciedade, que também demonstrou melhorar ou reverter a resistência à insulina na cetoacidose diabética ou resistência à insulina hepática induzida pela dieta, pode estar envolvida. [42,44] A secreção de leptina é regulada negativamente em adipócitos expostos a um pH médio baixo, enquanto a administração de bicarbonato de sódio a pessoas com acidose induzida por rins aumenta os níveis séricos de leptina. [45,46] Assim, a desregulação da leptina também pode ser causada por acidose que leva à resistência à insulina. [26]
Um estudo duplo-cego randomizado em 153 mulheres e homens saudáveis com 50 anos ou mais deu bicarbonato de potássio, bicarbonato de sódio ou placebo para verificar se ocorreriam alterações na insulina ou glicose em jejum. [47] O estudo durou apenas 84 dias, mas não mostrou alterações significativas nesses marcadores. Assim, este estudo clínico humano aparentemente contradiz os estudos anteriores que mostram que a terapia alcalina melhora a sensibilidade à insulina.
No entanto, para que a terapia alcalina funcione, a população de pacientes deve ter acidose metabólica de baixo grau na linha de base, caso contrário, não há acidose para melhorar. É provável que esta tenha sido uma limitação fundamental do estudo. Por exemplo, os grupos placebo, potássio e bicarbonato de sódio tiveram um pH urinário basal que era apenas limítrofe para retenção ácida (6,3, 6,04 e 6,12, respectivamente).
Esses níveis de pH urinário também são muito maiores do que um pH urinário <5,3, que é necessário para o diagnóstico de acidose metabólica. Adicionalmente, o grupo placebo aparentemente teve menos acidose na linha de base versus aqueles que receberam bicarbonato de potássio e sódio, pois tinham um pH urinário mais alto (ou seja, 6,3 versus 6,04 e 6,12, respectivamente). Em outras palavras, o grupo placebo parecia ser mais alcalino no início do estudo do que os grupos que receberam terapia alcalina. Estas são provavelmente as razões pelas quais o estudo não mostrou benefícios na glicemia ou insulina em jejum.
Talvez ainda mais importante, os autores também notaram que suas descobertas podem ter sido devido ao acaso, e que a medida que eles usaram para determinar a resistência à insulina não era muito precisa, como observado a seguir, ‘… observadas diferenças, é possível que, devido ao acaso, não tenhamos detectado efeitos verdadeiros e clinicamente significativos do tratamento com bicarbonato em nossos resultados.
Em segundo lugar, HOMA-IR é um índice relativamente bruto de resistência à insulina em comparação com métodos mais elaborados.’ [47] De fato, usar glicose e insulina em jejum não é uma maneira muito boa de medir a resistência à insulina. 64% das pessoas com testes orais normais de tolerância à glicose apresentam testes anormais de insulina pós-prandial indicativos de resistência à insulina ou diabetes tipo 2. [48]
Assim, estudos futuros precisam ser feitos em indivíduos com graus variados de acidose metabólica (pH urinário baixo, bicarbonato sérico baixo, citrato urinário baixo, amônio urinário alto) e melhores marcadores de resistência à insulina, como dosagem de insulina pós-prandial ou glicemia padrão-ouro A técnica de pinçamento deve ser empregada. [26]
No entanto, um desses estudos já foi realizado. De fato, ao usar a técnica de clamp hiperglicêmico e euglicêmico (o padrão-ouro para medir a resistência à insulina), a indução experimental de acidose metabólica provou induzir a intolerância à glicose.[32] De fato, a acidose metabólica causou uma diminuição significativa na sensibilidade tecidual à insulina em 32% e na sensibilidade tecidual à insulina exógena em 15%. Os níveis de insulina em jejum também aumentaram, apesar das concentrações normais de glicose, indicando resistência à insulina.
Esses danos ocorreram quando o pH do sangue diminuiu de 7,42 para 7,37, que ainda é considerado um pH sanguíneo normal (7,35-7,45). No entanto, o bicarbonato sérico diminuiu de 24 para 19 mEq/L (abaixo da faixa normal de bicarbonato, 23-29 mEq/L, indicando acidose metabólica de baixo grau).
Para resumir, estudos em humanos confirmaram que a indução de acidose metabólica de baixo grau induz resistência à insulina usando as técnicas de fixação de glicose padrão-ouro e que a correção dessa acidose metabólica melhora a sensibilidade à insulina.[ 31,32]
Resumo dos efeitos da acidose na resistência à insulina
-
A indução experimental de acidose metabólica em humanos prejudica o metabolismo da glicose e a sensibilidade celular à insulina. [32]
-
A correção da acidose metabólica em humanos melhora a sensibilidade à insulina.[31]
-
A acidose metabólica reduz a ligação da insulina aos receptores nos adipócitos e induz a resistência à insulina no músculo [14,34,35]
-
A acidose metabólica aumenta a produção de cortisol, o que reduz a sensibilidade à insulina no músculo esquelético e nas células adiposas.[26]
-
A acidose metabólica leve reduz a ligação da insulina ao seu receptor e a sinalização intracelular da insulina a jusante nos mioblastos e adipócitos.[14,35,39]
-
Um pH baixo diminui a expressão do sensibilizador de insulina adiponectina, [40] que é um hormônio que melhora a sensibilidade à insulina do músculo esquelético. [26,41]
-
A secreção de leptina é regulada negativamente em adipócitos expostos a um pH médio baixo, enquanto a administração de bicarbonato de sódio a pessoas com acidose induzida por rins aumenta os níveis séricos de leptina.[45,46]
Referências
James J DiNicolantonio and James H O’Keefe